STTT | 心肌I/R损伤研究新突破!ZBP1介导泛凋亡成核心靶点,一站式科研支撑助力机制解析
核心发现:ZBP1是心肌I/R损伤的核心调控靶点

1
细胞特异性表达,心肌细胞是唯一核心载体
研究通过I/R损伤小鼠模型转录组分析,并与已发表ICM (ischemic cardiomyopathy)患者的RNA-seq数据集进行交叉分析,结合模型小鼠原代心肌细胞与非心肌细胞的分离验证,发现ZBP1仅在心肌细胞中显著高表达,成纤维细胞、内皮细胞、免疫细胞等无显著变化,且其上调独立于经典cGAS-STING通路,明确了ZBP1的心肌细胞特异性作用。
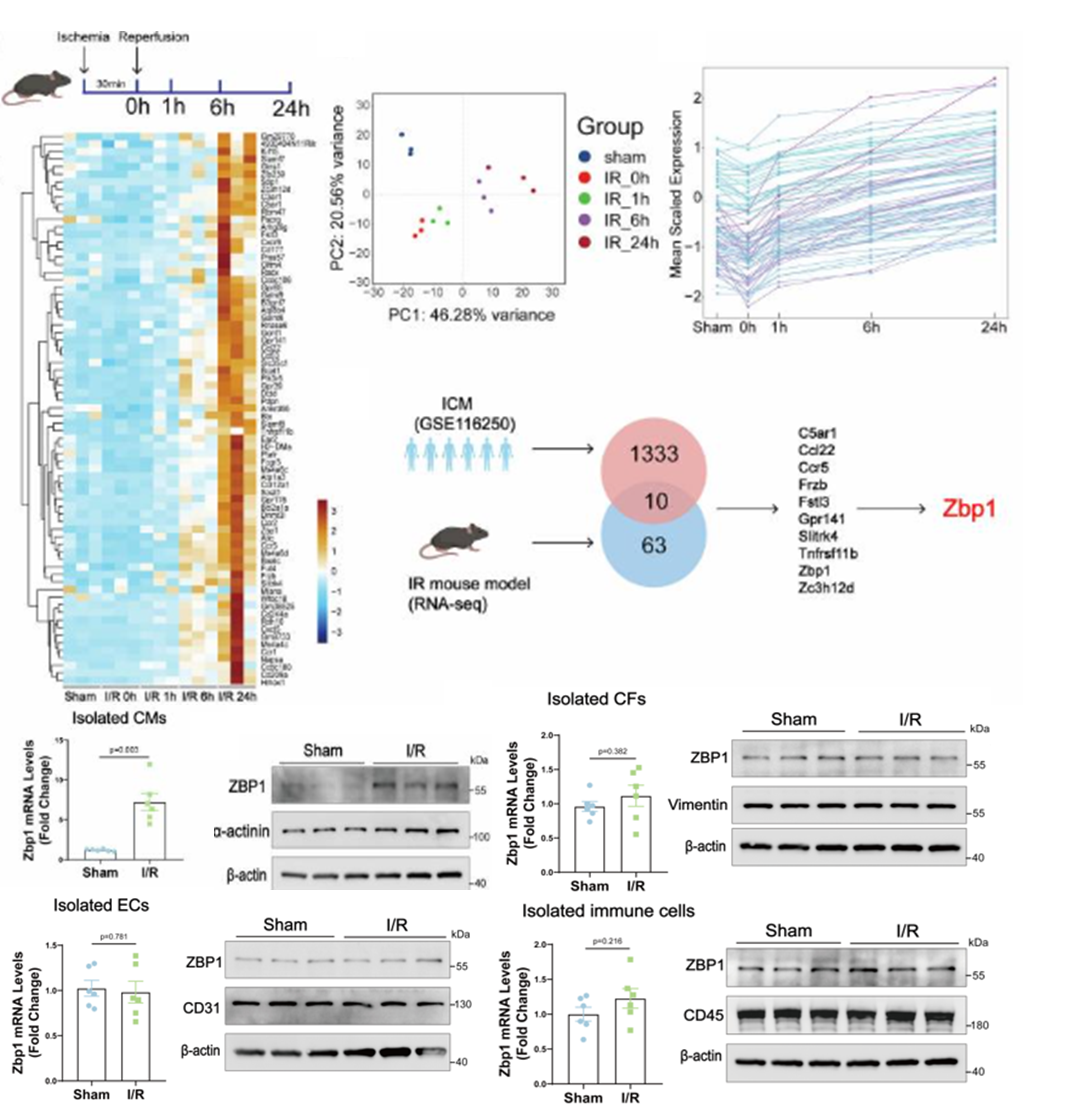
图2 生物信息学分析确定了ZBP1在心肌I/R损伤中的关键作用并验证在心肌细胞中特异表达
驱动泛凋亡,干预效果优于传统单一抑制剂
2
构建心肌细胞特异性ZBP1敲除/过表达小鼠模型证实:ZBP1缺失可显著抑制心肌细胞焦亡、凋亡、坏死性凋亡的协同发生(泛凋亡),缩小心肌梗死面积的效果远超坏死性凋亡抑制剂GSK’872、泛Caspase抑制剂z-VAD-FMK;而ZBP1过表达可直接诱导心肌细胞泛凋亡、心脏重构甚至心力衰竭。
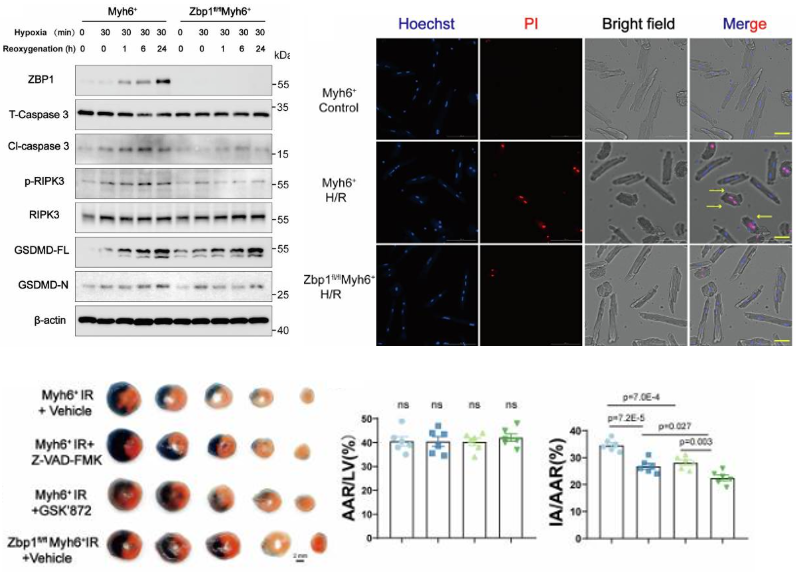
图3 ZBP1缺乏显著抑制心肌细胞泛凋亡且比GSK'872和zVAD缩小的梗塞区域更大
3
解析分子机制,组装非经典泛凋亡小体
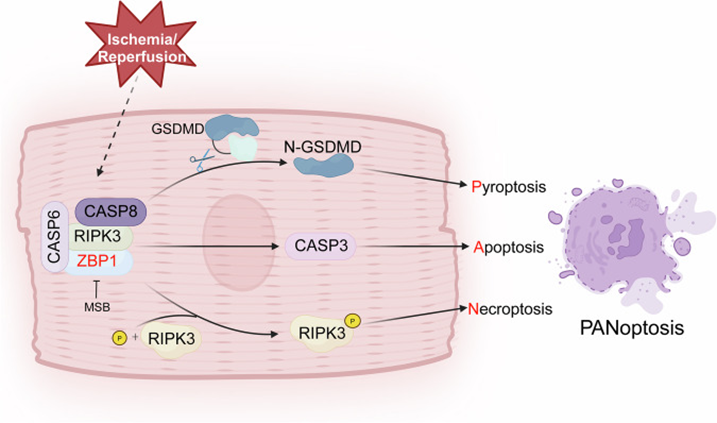
免疫共沉淀、免疫荧光等实验证实,ZBP1通过与RIPK3、CASP8、CASP6形成心肌细胞特异性非经典泛凋亡小体驱动泛凋亡,该复合物无经典组分RIPK1、NLRP3等,是心肌细胞死亡的核心分子结构。
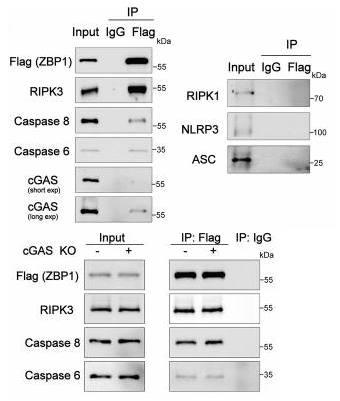
图4 ZBP1、RIPK3、CASP8和CASP6之间相互作用
靶向抑制剂MSB,有效改善心肌I/R损伤
4
通过虚拟药物筛选获得的ZBP1抑制剂MSB,可高亲和力结合ZBP1并阻断泛凋亡小体组装,体内外实验均证实其能显著缓解心肌细胞死亡、缩小心肌梗死面积、改善心脏功能,展现出良好的治疗潜力。
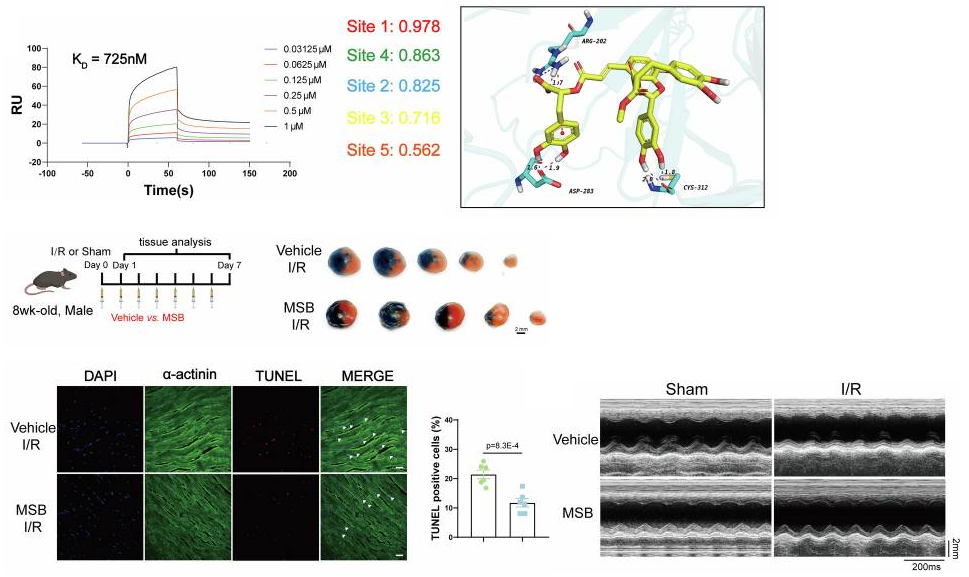
图5 MSB对固定的ZBP1蛋白表现强的结合反应并可预防心肌缺血再灌注损伤
研究意义:为心血管研究与治疗开辟新方向
该研究聚焦成年心肌细胞,阐明了ZBP1介导泛凋亡的核心作用,突破了传统靶向单一细胞死亡通路的局限,为心肌I/R损伤、心梗、心力衰竭等疾病提供了全新的心肌细胞特异性治疗靶点,而MSB的发现也为临床药物研发奠定了基础。同时,研究再次验证了原代心脏细胞分离培养和多维度实验技术融合在心血管研究中的核心价值。优质的科研材料、标准化的实验模型、专业的技术服务,是解锁心血管疾病分子机制、加速靶向药物研发的关键。
研究背后:优质科研工具与技术支撑是关键
本次研究的所有核心结论,均建立在高纯度原代心脏细胞分离培养和细胞-动物水平的双重验证之上:
1. 原代心肌/内皮/成纤维细胞的精准分离,是明确ZBP1细胞特异性的前提,避免了非靶细胞的实验干扰;
2. 原代心肌细胞缺氧/复氧模型,为体外验证ZBP1的功能与机制提供了贴近体内生理状态的实验体系;
3. 心肌I/R小鼠模型构建、超声心动图检测、心肌梗死面积定量等小动物实验,完成了从体外机制到体内药效的关键验证;
4. 免疫共沉淀、qRT-PCR、Western Blot等分子实验,清晰解析了ZBP1介导泛凋亡的分子通路。
而这些核心技术,正是心血管疾病基础研究与药物研发的必备支撑,也是百洋智心深耕的核心领域。心血管研究整体解决方案——试剂盒+技术服务双管齐下,覆盖原代心脏细胞培养、疾病模型构建、分子机制解析、药物初筛全流程,大幅提升科研效率,加速课题成果产出!


百洋智心基础研究技术平台
提供分子生物(WB/IP/荧光染色)、细胞实验(模型构建/功能检测)、小动物模型(心梗模型构建+超声检测+饲养)一站式实验服务,专业团队助力科研高效推进!

百洋智心专注心血管研究领域,以原代心肌/内皮/成纤维细胞分离培养试剂盒为核心,搭配分子、细胞、小动物全流程实验服务,为广大科研工作者提供高性价比的科研解决方案,助力心血管研究课题快速突破!

微信扫码咨询客服



哔哩哔哩丨百洋智心
咨询热线丨010-60855551

本篇文章来源于微信公众号:百洋智心